방문해 주셔서 감사합니다.
SEARCH
식약처 인증
임상시험
의료기기
신청자료
임상시험(변경 계획승인신청서)
1.임상시험계획서 또는 임상시험변경계획서
2. 임상시험용 의료기기가 필요 2의 제조소의 시설기준에 적합한 시설에서 제조되고 있음을 입증하는 자료
3. 의료기기법 시행규칙 제 2항의 규정에 의한 기술문서 등에 관한 자료
* 기술문서에 관한 자료
- 사용목적에 관한 자료
- 물리, 화학적 특성에 관한 자료
- 전기, 기계적 안전에 관한 자료
- 생물학적 안전에 관한 자료
- 방사선에 관한 안전성 자료
- 전자파장해에 관한 자료
- 성능에 관한 자료
- 제품의 성능 및 안전을 확인하기 위한 시험규격 및 그 설정근거와 실측치에 관한 자료
* 안전성, 유효성에 관한 자료
다만, 이미 허가를 받은 품목과 구조, 원리, 성능, 사용목적 및 사용방법 등이 본질적으로 동등한 품목의 경우에는 이를 생략할 수 있다.
- 기원 또는 발견 및 개발경위에 관한 자료
- 안전성에 관한 자료
- 임상시험에 관한 자료
- 외국의 사용현황 등에 관한 자료
- 국내 유사제품과 비료, 검토한 자료 및 당해 의료기기의 특성에 관한 자료
- 임상시험실시기관의 승인서
임상시험 계획서
1. 임상시험의 명칭
2. 임상시험의 실시기관의 명칭 및 소재지
3. 임상시험의 책임자, 담당자 및 공동연구자의 성명 및 작명
4. 임상시험용 의료기기를 관리하는 관리자의 성명 및 작명
5. 임상시험 의뢰자의 성명 및 주소
6. 임상시험의 목적 및 배경
7. 임상시험용 의료기기의 사용목적(대상질환 또는 적응증을 포함)
8. 피험자의 선정기준, 제외기준, 인원 및 그 근거
9. 임상시험기간
10. 임상시험방법 (사용량, 사용방법, 사용기간, 병용요법 등을 포함)
11. 관찰항목, 임상검사항목 및 관찰검사방법
12. 예측되는 부작용 및 사용시 주의사항
13. 중지, 탈락기준
14. 성능의 평가기준, 평가방법 및 해석방법 (통계분석방법에 의함)
15. 부작용을 포함한 안전서의 평가기준, 평가방법 및 보고방법
16. 피험자 동의서 서식
17. 피해자 보상에 대한 규약
18. 임상시험 후 피험자의 진료에 관한 사항
19. 피험자의 안전보호에 관한 대책
20. 그 밖에 임상시험을 안전하고 과학적으로 실시하기 위하여 필요한 사항
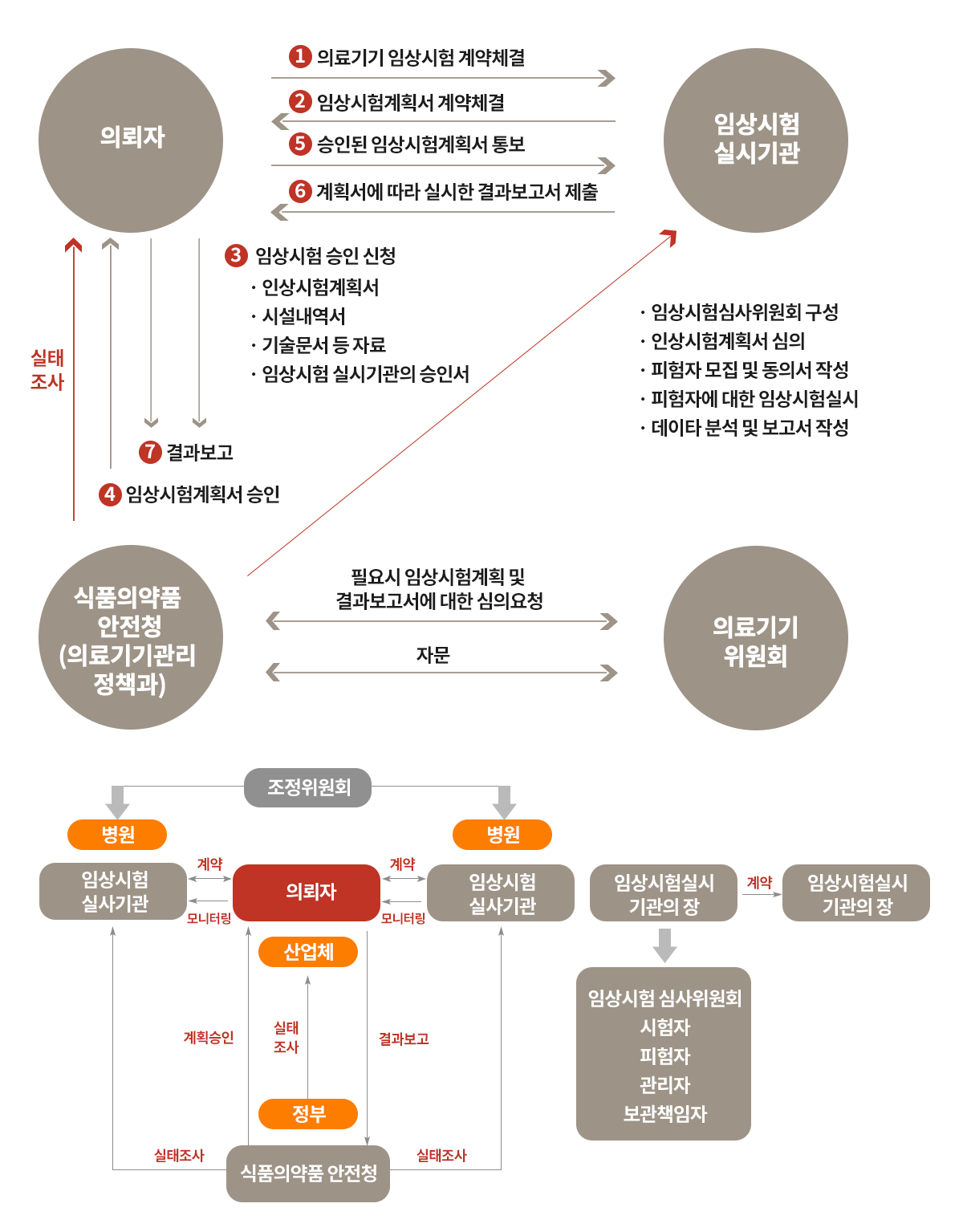
임상시험 계획 승인